Тепловое движение частиц, находящихся в узлах кристаллической решетки сводится к колебаниям около своих положений равновесия – узлов решетки. Эти колебания можно разложить на три взаимно перпендикулярных направления. Таким образом, каждой частице, составляющей кристаллическую решетку, присваивают три колебательных степени свободы, каждая из которых согласно закону распределения энергии по степеням свободы обладает энергией ![]() .
.
Внутренняя энергия одного моля твердого тела равна:
![]() ,
,
где Na – число Авогадро; k – постоянная Больцмана; Nak = R – универсальная газовая постоянная.
Молярная теплоемкость твердого тела равна:
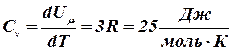 . (9.8)
. (9.8)
Формула (9.8)выражает закон Дюлонга и Пти: молярная (атомная) теплоемкость химически простых тел в кристаллическом состоянии одинакова (равна 3R) и не зависит от температуры.
Если твердое вещество является химическим соединением (например, NaCl), то молярная теплоемкость равна:
![]() ,
,
где n – число атомов в молекуле.
При низких температурах теплоемкость твердых тел зависит от температуры: Cv ~ Т3 .