Наибольшее количество диоксида серы (после выбросов от сгорания топлива, составляющих более 10 % общего количества выделяющегося SO2) выделяется в процессах обжига и переработки сульфидных руд меди, свинца и цинка. Имеются производства, которые выбрасывают в атмосферу газы, содержащие около 4 – 10 % SO2, что является достаточным для организации производства серной кислоты. Этому мешает лишь удаленность предприятия по первичной обработке руд цветных металлов от районов, где серная кислота могла бы применяться для производства удобрений или в химических процессах.
Отмечено, например, что Австралия, импортирующая серу для производства сельскохозяйственных удобрений, могла бы обеспечить себя собственным сырьем, используя серосодержащие отходы, образующиеся в металлургическом производстве.
Выходящие из плавильных печей (особенно медных) газы, содержащие SО2, оказывают опасное воздействие на растительность. Гибель растительности, сопровождающаяся эрозией почв, привела к появлению пустынных районов, типичных для Дактауна, Теннеси, Квинстоуна, Тасмании и др., где из печей для выплавки меди и других цветных металлов в атмосферу выбрасывали газы без очистки.
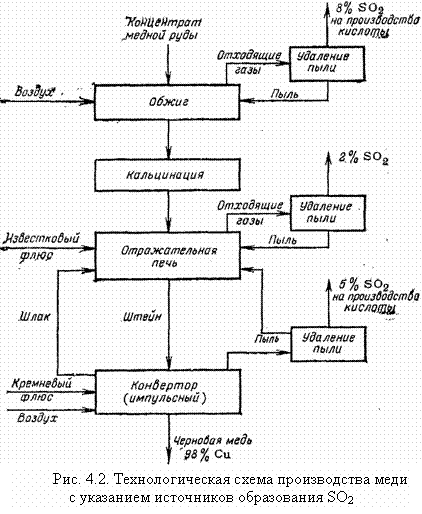
В процессе выплавки меди (рис. 4.2), руда подвергается первичному окислительному обжигу для частичного удаления серы; при этом концентрация ее в отходящих газах составляет около 8 %. Продукт обжига представляет собой смесь сульфидов и оксидов меди и железа. Его направляют одновременно с известняком или кремнеземом в качестве флюса в отражательную печь, где он взаимодействует с оксидами металлов и другими примесями. При этом на поверхность расплава всплывают сульфиды меди и железа, образуя штейн. Отходящие газы содержат 1 – 2 % SO2. Для поглощения SO2 требуются специальные методы.
Штейн затем нагревают в конверторе, где одновременно с окислением железа происходит окисление оставшейся серы до диоксида, концентрация которого в отходящих газах составляет около 3 – 5 %. В целом получение меди можно описать следующими химическими реакциями:
2 Cu2S + 3 O2![]() 2 Cu2O + 2 SO2
2 Cu2O + 2 SO2
2 Cu2O + Cu2S ![]() 6 Cu + S O2
6 Cu + S O2
 |
Свинец и цинк чаще всего получают из сульфидных минералов галенита (PbS) и цинковой обманки (ZnS), которые обычно присутствуют вместе.
Руду подвергают обжигу в печи с движущейся решеткой, либо в печи с псевдоожиженным слоем. Отходящие газы, содержащие до 6 % SO2, используют, когда это возможно, для производства серной кислоты. В этом случае главной проблемой является содержание в выходящих из обжиговых печей газах триоксида мышьяка (As2O3), хлористого водорода (HCl), фтористого водорода (HF) и других примесей, являющихся катализаторными ядами.
Они мешают протеканию стадии каталитического окисления, поэтому их необходимо удалять из газового потока вместе с примесями твердых частиц. При получении цинка, кроме SO2, выделяется и угарный газ:
ZnS + 3/2 O2 > ZnO + SO2
ZnO + C > Zn + CO