Числом степеней свободы механической системы называется количество независимых величин, с помощью которых может быть задано положение системы. Молекулу одноатомного газа можно представить материальной точкой, которой приписывают три степени свободы поступательного движения (рис. 7.7, а). Молекулу двухатомного газа можно рассматривать как совокупность двух материальных точек, жестко связанных между собой (рис. 7.7, б). Эта система, кроме трех поступательных степеней свободы, имеет еще две вращательные – всего пять степеней свободы: ![]() .
.
Трехатомная и многоатомные молекулы имеют три поступательных и три вращательных степени свободы – всего шесть: ![]() (рис. 7.7, в).
(рис. 7.7, в).
 Молекулы реальных газов обладают еще степенями свободы колебательного движения. Больцман сформулировал закон распределения энергии молекул газа по степеням свободы.
Молекулы реальных газов обладают еще степенями свободы колебательного движения. Больцман сформулировал закон распределения энергии молекул газа по степеням свободы.
Для статистической системы, находящейся в состоянии термодинамического равновесия, на каждую поступательную и вращательную степень свободы приходится в среднем кинетическая энергия, равная ![]() , а на каждую колебательную степень свободы – в среднем энергия, равная
, а на каждую колебательную степень свободы – в среднем энергия, равная ![]() .
.
Средняя энергия молекулы равна: ![]() , где
, где ![]() для идеального газа. Энергия одного моля газа:
для идеального газа. Энергия одного моля газа:
![]() . (7.16)
. (7.16)
Энергия любой массы газа:
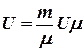 ;
; 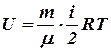 . (7.17)
. (7.17)
Здесь 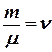 – количество вещества, поэтому выражение (7.17) можно записать в виде
– количество вещества, поэтому выражение (7.17) можно записать в виде
![]() .
.