Между термодинамическими параметрами ![]() и
и ![]() существует связь, называемая уравнением состояния, которое в общем виде записывается уравнением:
существует связь, называемая уравнением состояния, которое в общем виде записывается уравнением:
![]() .
.
В соответствии с законами Бойля-Мариотта и Гей-Люссака уравнение состояния имеет вид:
![]() .
.
Уравнение Клапейрона-Менделеева для одного моля газа имеет вид:
![]()
Здесь ![]() - объем одного моля газа, R = 8,31 Дж/моль К – универсальная газовая постоянная. Для любой массы (m) газа уравнение Клапейрона-Менделеева имеет вид:
- объем одного моля газа, R = 8,31 Дж/моль К – универсальная газовая постоянная. Для любой массы (m) газа уравнение Клапейрона-Менделеева имеет вид:
 , или
, или ![]() , (7.1)
, (7.1)
где 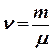 – количество вещества,
– количество вещества, ![]() - молярная масса газа.
- молярная масса газа.
Другая форма уравнения Клапейрона- Менделеева:
![]() . (7.2)
. (7.2)
Здесь n =N/V – концентрация молекул (число молекул в единице объема), k = R/NA – постоянная Больцмана. Так как число Авогадро ![]() - число молекул в одном моле любого вещества, то
- число молекул в одном моле любого вещества, то ![]() .
.